1. Hội chứng tăng đông thrombophilia là gì?
Thrombophilia, hội chứng tăng đông máu, chỉ tình trạng mà một người dễ hình thành các huyết khối (cục máu đông) trong tĩnh mạch và động mạch, là hệ quả của yếu tố di truyền hoặc các yếu tố mắc phải, hoặc cả hai. Người gặp phải tình trạng này sẽ bị tăng nguy cơ bệnh huyết khối tĩnh mạch (Venous Thromboembolism – VTE); VTE có rất nhiều dạng khác nhau nhưng phần lớn các trường hợp có thể chia làm hai dạng phổ biến:
– Huyết khối tĩnh mạch sâu (Deep Vein thrombosis – DVT): thường gây ra các cơn đau nhức tại các vùng mạch máu ở sâu trong lớp biểu bì.
– Tắc mạch phổi hay thuyên tắc phổi (Pulmonary embolism – PE): gây ra các bệnh thứ phát liên quan đến đường hô hấp .
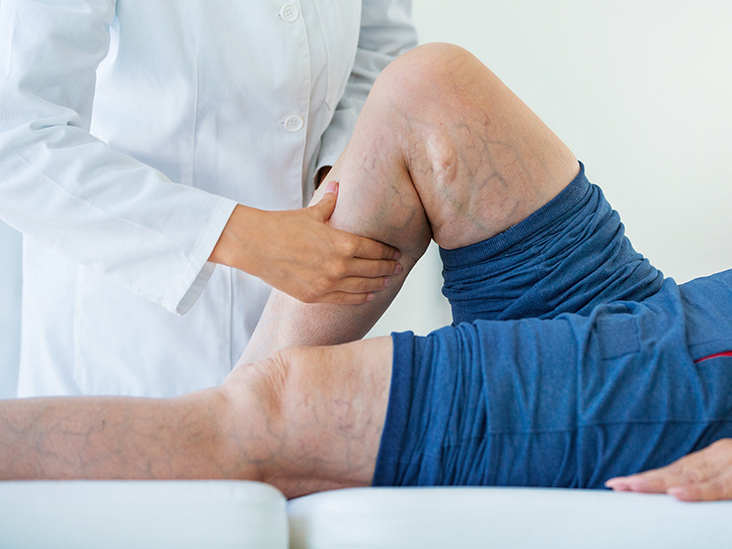
Người bệnh cần chú ý rằng ngoài gây bệnh huyết khối, trạng thái tăng đông có thể tăng nguy cơ xơ vữa động mạch, bệnh động mạch là nguyên nhân của nhồi máu cơ tim và các dạng bệnh tim mạch khác.[12, 13]
Tình trạng rối loạn tăng đông máu còn là nguyên nhân phổ biến nhất gây ra sự phát triển bệnh thuyên tắc huyết khối trong thai kỳ và từ đó dẫn tới nhiều bệnh lý như: thai chậm phát triển, các dạng nghiêm trọng của việc bong nhau thai sớm và tiền sản giật, thai lưu, sảy thai liên tiếp.
Cơ chế bệnh
Quá trình đông máu thông thường chỉ được diễn ra tại mô bị tổn thương, tại đó giải phóng các chất gây đông máu. Các chất này bám vào các yếu tố đông máu có trong máu như yếu tố VII, X và IX. Yếu tố X thúc đẩy tiền chất của thrombin (prothrombin) thành prombin; thrombin là enzyme trung tâm của quá trình đông máu: nó kích hoạt protein sợi huyết (fibrin) và các enzyme đông máu khác gồm yếu tố V, VIII và TAFI để hình thành cục máu đông.
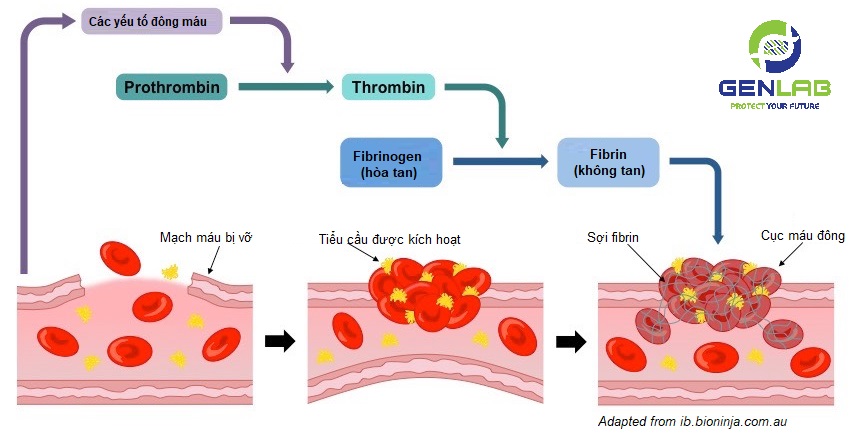
Quá trình đông máu bị kiềm chế bởi một số protein như antithrombin, protein C, protein Z để giữ cho quá trình đông máu chỉ diễn ra ở mức độ cần thiết.
Trong hộii chứng tăng đông thrombophilia, sự cân bằng giữa hoạt động của chất gây đông và chất chống đông bị phá vỡ. Sự bất thường về hoạt động của các protein này, dù không đáng kể, ví dụ sự giảm chất antithrombin còn 70 – 80% mức bình thường, cũng có thể tăng nguy cơ bệnh huyết khối.
2. Nguyên nhân của hội chứng tăng đông máu thrombophilia
Thrombophilia có thể do bẩm sinh hoặc mắc phải. Tăng đông bẩm sinh thường là do di truyền và có thể gọi là bệnh huyết khối di truyền, làm tăng xu hướng phát triển huyết khối. Trong khi đó, tăng đông mắc phải liên quan đến các bệnh phát sinh trong đời sống của mỗi người, thường thể hiện rõ ở độ tuổi trưởng thành.
Bẩm sinh
Hội chứng tăng đông thrombophila bẩm sinh phổ biến nhất là những dạng phát sinh do hoạt động quá mức của các yếu tố đông máu. Những yếu tố phổ biến nhất là yếu tố V Leiden (đột biến gen FV ở vị trí 1691) và prothrombin G20210A (đột biến ở prothrombin ở vị trí 20210 của gen).[1, 6] Bệnh huyết khối di truyền do đột biến yếu tố V Leiden chiếm khoảng 5% ở châu Âu, trong khi đột biến G20210A có ở 2% dân số. Các trường hợp này thường gây ảnh hưởng nhẹ.
Các dạng hiếm gặp của bệnh huyết khối bẩm sinh thường do thiếu các chất chống đông máu tự nhiên. Trường hợp này có khuynh hướng gây huyết khối nặng hơn.[5] Những nguyên nhân chính bao gồm thiếu antithrombin III (ATIII, serpin), thiếu protein C và thiếu protein S.[1, 6] Bệnh huyết khối hiếm gặp hơn là đột biến yếu tố XIII[6] và rối loạn protein tiêu sợi huyết có tính gia đình (fibrinogen bất thường).[6]
Nhóm máu có thể cũng liên quan đáng kể đến nguy cơ gây ra hội chứng rối loạn đông máu thrombophilia. Những người có nhóm máu không phải nhóm O có nguy cơ cao gấp 2 – 4 lần. Nhóm máu O có liên quan đến giảm nồng độ yếu tố von Willebrand và yếu tố VIII, hai yếu tố có liên quan đến nguy cơ bệnh huyết khối.[4]

Mắc phải
Một số bệnh mắc phải làm tăng nguy cơ bệnh huyết khối. Một ví dụ nổi bật là hội chứng kháng phospholipid,[1, 6] do các kháng thể chống lại các thành phần của màng tế bào, đặc biệt là lupus anticoagulant, kháng thể kháng cardiolipin và kháng thể kháng β2-glycoprotein 1; do đó kháng lipid được coi là một bệnh tự miễn. Trong một số trường hợp, hội chứng kháng phospholipid có thể gây huyết khối động mạch cũng như tĩnh mạch, có liên quan chặt chẽ hơn đến sảy thai.[6]
Giảm tiểu cầu do heparin (HIT) là do phản ứng của hệ thống miễn dịch chống lại thuốc chống đông máu heparin (hoặc các dẫn xuất của nó).[1] HIT làm tăng nguy cơ huyết khối tĩnh mạch và động mạch.[7] Huyết sắc tố niệu kịch phát về đêm (PNH) là một tình trạng hiếm gặp do những thay đổi trong gen PIGA, gen này có vai trò bảo vệ tế bào máu khỏi hệ thống bổ thể. PNH làm tăng nguy cơ hình thành huyết khối tĩnh mạch đồng thời cũng có liên quan đến thiếu máu tán huyết.[8]
Ngoài ra, bệnh hồng cầu hình liềm (do đột biến của hemoglobin) được coi là một dạng bệnh huyết khối nhẹ do suy giảm tuần hoàn máu.[1] Tương tự, rối loạn tăng sinh tủy, trong đó tủy xương tạo ra quá nhiều tế bào máu, dẫn đến hình thành huyết khối, đặc biệt là trong bệnh đa hồng cầu (thừa hồng cầu) và tăng tiểu cầu thiết yếu (thừa tiểu cầu).
Ung thư, nhất là khi di căn, là một yếu tố nguy cơ đối với huyết khối.[2, 6]
Phụ nữ mang thai cũng tăng nguy cơ bị bệnh huyết khối. Điều này có thể là kết quả của tình trạng tăng đông máu sinh lý trong thai kỳ để bảo vệ khỏi xuất huyết sau sinh.[9]
Nội tiết tố nữ estrogen, khi được sử dụng trong viên uống tránh thai kết hợp và trong liệu pháp thay thế hormone tiền mãn kinh, có thể làm tăng nguy cơ huyết khối tĩnh mạch gấp 2 – 6 lần.[10]
Béo phì cũng được coi là một yếu tố nguy cơ của bệnh rối loạn tăng đông máu (làm tăng hơn gấp đôi nguy cơ), nhất là khi người bệnh có sử dụng thuốc tránh thai hoặc trong thời gian sau phẫu thuật. Nhiều bất thường về đông máu khác nhau đã được mô tả ở người béo phì. Ở những người này có nồng độ cao hơn của chất ức chế hoạt hóa plasminogen-1 (PAI-I/Serpin E1), một chất gây tăng đông.[11]
Chưa rõ nguyên nhân
Một số tình trạng có liên quan đến thrombophilia có thể do di truyền hoặc mắc phải.[6] Các tình trạng đó bao gồm: tăng lượng protein yếu tố VIII, yếu tố IX, XI, fibrinogen và thrombin-activatable fibrinolysis inhibitor (TAFI) … Kháng protein C hoạt hóa không do đột biến yếu tố V thì có thể do các yếu tố khác gây ra và vẫn là một nguy cơ của bệnh huyết khối.[6]
Ngoài ra, các bác sĩ đang nghi vấn về mối quan hệ giữa lượng homocysteine trong máu và bệnh huyết khối.[6] Mức độ homosysteine được xác định bởi các đột biến gen MTHFR và CBS, hoặc cũng có thể còn do lượng folic acid, vitamin B6 and vitamin B12 hấp thu vào cơ thể.[5]
3. Chẩn đoán và sàng lọc hội chứng tăng đông thrombophilia
Chẩn đoán tăng đông thrombophilia
Thrombophilia có thể được chẩn đoán dựa vào xét nghiệm sinh hóa máu.
Các xét nghiệm cho tình trạng thrombophilia là các xét nghiệm định lượng nồng độ hoặc hoạt tính của các yếu tố tham gia vào quá trình đông máu, bao gồm đếm tế bào tổng số, thời gian prothrombin, thời gian prothrombin từng phần, thời gian thrombin và thời gian reptilase, chống đông lupus, v.v… [2] Từ kết quả xét nghiệm trên, dựa vào cơ chế bệnh để chẩn đoán tình trạng bệnh huyết khối.
Để các kết quả chính xác cho hội chứng tăng đông thrombophilia, các xét nghiệm sinh hóa cần thực hiện vài tuần hoặc vài tháng sau khi bệnh nhân trải qua đợt huyết khối tĩnh mạch hoặc thuyên tắc phổi, vì các tình trạng này có thể ảnh hưởng tới kế quả xét nghiệm (thrombophilia và bệnh huyết khối không hẳn là một, trong khi chúng ta đang muốn chẩn đoán tình trạng thrombophilia). Thường thì bệnh nhân sẽ phải chờ đến khi thuốc làm loãng máu (thuốc chống đông máu) như warfarin, hết tác dụng – có thể cần 4 – 6 tuần. Nếu người cần xét nghiệm gần đây có mang thai, xét nghiệm cần phải trì hoãn đến 8 tuần sau khi sinh, bởi hiện tượng tăng đông sinh lý ở thai phụ làm sai lệch kết quả.
Các phương pháp chẩn đoán hình ảnh có thể được sử dụng để phát hiện xem bệnh nhân có các cục máu đông bất thường hay không: siêu âm Doppler, chụp cộng hưởng từ, chụp tĩnh mạch (MRI), chụp vi tính cắt lớp (CT), quét thông khí/tưới máu.
Sàng lọc tăng đông di truyền
Tăng đông di truyền chủ yếu rơi vào hai nhóm: trạng thái nguy cơ huyết khối thấp, ví dụ như trường hợp kháng protein C hoạt hóa (do đột biến yếu tố V Leiden) và trạng thái nguy cơ huyết khối cao hiếm, bao gồm thiếu protein C, S. Những gen sau đây được khuyến nghị đưa vào xét nghiệm sàng lọc:
- Gen yếu tố V Leiden (F5, đột biến G1691A)[15]
- Gen yếu tố II (Prothrombin, đột biến G20210A)[16]
- Gen MTHFR (đột biến C677T)
- Gen antithrombin, protein C, S
Những ai nên cân nhắc xét nghiệm bệnh rối loạn tăng đông di truyền
Xin lưu ý: Xét nghiệm sàng lọc bệnh huyết khối di truyền KHÔNG được chỉ định ở những bệnh nhân KHÔNG gặp phải tình trạng huyết khối tĩnh mạch.[17]
(A) Bệnh nhân có các triệu chứng của bệnh tăng huyết khối
Khuyến cáo nên thực hiện tầm soát bệnh huyết khối ở những bệnh nhân sau[18]:
- Thuyên tắc huyết khối tĩnh mạch không rõ nguyên nhân trước 40 tuổi
- Người gặp phải các đợt huyết khối tắc mạch không rõ nguyên nhân
- Huyết khối ở các vị trí bất thường
- Thuyên tắc huyết khối tĩnh mạch không rõ nguyên nhân ở bệnh nhân có người thân trực hệ rơi vào trường hợp 1-3 kể trên
- Phụ nữ bị sẩy thai muộn không rõ nguyên nhân hoặc sẩy thai sớm tự phát ≥3 lần
- Hoại tử da không rõ nguyên nhân, đặc biệt nếu dùng thuốc đối kháng vitamin K (ví dụ: Warfarin)
- Trẻ em và trẻ sơ sinh xuất hiện ban xuất huyết bạo phát
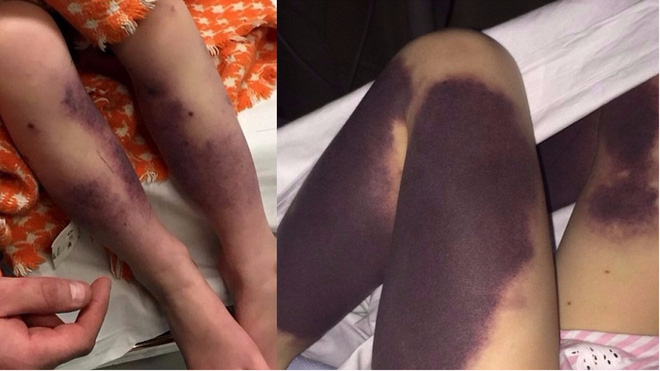
(B) Người thân trực hệ KHÔNG có triệu chứng bệnh huyết khối[18]
Xét nghiệm sàng lọc huyết khối di truyền cũng nên cân nhắc dành cho người thân ở độ tuổi trưởng thành (anh chị em, cha mẹ, con cái ≥16 tuổi) của bệnh nhân có tiền sử huyết khối tĩnh mạch.
Xác định sớm nguy cơ bệnh huyết khối cho các thành viên trong gia đình có thể tạo cơ hội cho việc điều trị đích ngắn hạn trong các giai đoạn tăng nguy cơ huyết khối (ví dụ: phẫu thuật, chấn thương, …).
4. Điều trị cho hội chứng tăng đông thrombophilia
Không có phương pháp điều trị cụ thể nào cho tình trạng tăng đông máu thrombophilia.
Ở những người bị huyết khối không rõ nguyên nhân và/hoặc tái phát nhiều lần, hoặc những người mang đột biến thrombophilia nguy cơ cao có thể cần phải sử dụng thuốc chống đông máu, chẳng hạn như warfarin, trong thời gian lâu dài để giảm nguy cơ gặp phải các đợt huyết khối tắc mạch tiếp theo.[3]
Những người bị hội chứng antiphospholipid có thể được chỉ định dùng thuốc kháng đông dài hạn sau đợt huyết khối vô căn đầu tiên.
Phụ nữ mắc chứng rối loạn đông máu đang dự tính mang thai hoặc đang mang thai thường không thể sử dụng warfarin trong thai kỳ, đặc biệt là trong 13 tuần đầu tiên, vì nó có thể tạo ra những bất thường ở thai nhi. Heparin trọng lượng phân tử thấp (LMWH, chẳng hạn như enoxaparin) thường được sử dụng thay thế.[14] Warfarin và LMWH có thể được sử dụng an toàn khi cho con bú.
Tài liệu tham khảo
[1] Mitchell RS, Kumar V, Abbas AK, Fausto N (2007). “Chapter 4”. Robbins Basic Pathology (Eighth ed.). Philadelphia: Saunders. ISBN 978-1-4160-2973-1.
[2] Heit JA (2007). “Thrombophilia: common questions on laboratory assessment and management”. Hematology Am. Soc. Hematol. Educ. Program. 2007 (1): 127–35. doi:10.1182/asheducation-2007.1.127. PMID 18024620.
[3] Kyrle PA, Rosendaal FR, Eichinger S (December 2010). “Risk assessment for recurrent venous thrombosis”. Lancet. 376 (9757): 2032–9. doi:10.1016/S0140-6736(10)60962-2. PMID 21131039. S2CID 31610364
[4] Rosendaal FR, Reitsma PH (July 2009). “Genetics of venous thrombosis”. J. Thromb. Haemost. 7 Suppl 1: 301–4. doi:10.1111/j.1538-7836.2009.03394.x. PMID 19630821.
[5] Crowther MA, Kelton JG (2003). “Congenital thrombophilic states associated with venous thrombosis: a qualitative overview and proposed classification system”. Ann. Intern. Med. 138 (2): 128–34. doi:10.7326/0003-4819-138-2-200301210-00014. PMID 12529095. S2CID 43161448. Lay summary.
[6] Rosendaal FR (2005). “Venous thrombosis: the role of genes, environment, and behavior”. Hematology Am. Soc. Hematol. Educ. Program. 2005 (1): 1–12. doi:10.1182/asheducation-2005.1.1. PMID 16304352.
[7] Keeling D, Davidson S, Watson H (May 2006). “The management of heparin-induced thrombocytopenia”. Br. J. Haematol. 133 (3): 259–69. doi:10.1111/j.1365-2141.2006.06018.x. PMID 16643427. Archived from the original on 2012-12-10.
[8] Brodsky RA (April 2008). “Narrative review: paroxysmal nocturnal hemoglobinuria: the physiology of complement-related hemolytic anemia”. Ann. Intern. Med. 148 (8): 587 95. CiteSeerX 10.1.1.668.4942. doi:10.7326/0003-4819-148-8-200804150-00003. PMID 18413620. S2CID 19715590.
[9] Bourjeily G, Paidas M, Khalil H, Rosene-Montella K, Rodger M (February 2010). “Pulmonary embolism in pregnancy”. Lancet. 375 (9713): 500–12. doi:10.1016/S0140-6736(09)60996-X. PMID 19889451. S2CID 8633455.
[10] Tchaikovski SN, Rosing J (July 2010). “Mechanisms of estrogen-induced venous thromboembolism”. Thromb. Res. 126 (1): 5–11. doi:10.1016/j.thromres.2010.01.045. PMID 20163835.
[11] Stein PD, Goldman J (September 2009). “Obesity and thromboembolic disease”. Clin. Chest Med. 30 (3): 489–93, viii. doi:10.1016/j.ccm.2009.05.006. PMID 19700047.
[12] Borissoff JI, Spronk HM, Heeneman S, ten Cate H (2009). “Is thrombin a key player in the ‘coagulation-atherogenesis’ maze?”. Cardiovasc. Res. 82 (3): 392–403. doi:10.1093/cvr/cvp066. PMID 19228706.
[13] Borissoff JI, Spronk HM, ten Cate H (2011). “The hemostatic system as a modulator of atherosclerosis”. N. Engl. J. Med. 364 (18): 1746–1760. doi:10.1056/NEJMra1011670. PMID 21542745.
[14] Bates SM, Greer IA, Pabinger I, Sofaer S, Hirsh J (June 2008). “Venous thromboembolism, thrombophilia, antithrombotic therapy, and pregnancy: American College of Chest Physicians Evidence-Based Clinical Practice Guidelines (8th Edition)”. Chest. 133 (6 Suppl): 844S–886S. doi:10.1378/chest.08-0761. PMID 18574280. Archived from the original on 2013-01-12.
[15] Franchini M (2012) Utility of testing for factor V Leiden. Blood Transfus 10(3):257–259.
[16] Poort SR. A common genetic variation in the 3’-untranslated region of the prothrombin gene is associated with elevated plasma prothrombin levels and an increase in venous thrombosis. Blood 88(10):3698–3703
[17] Baglin et al. (2009) British Committee for Standards in Haematology Guidelines: Page 1-19
[18] https://www.exeterlaboratory.com/test/thrombophilia-screening/
Tags: bệnh tăng đông máu, bệnh thrombophilia, huyết khối tĩnh mạch, rối loạn đông máu
